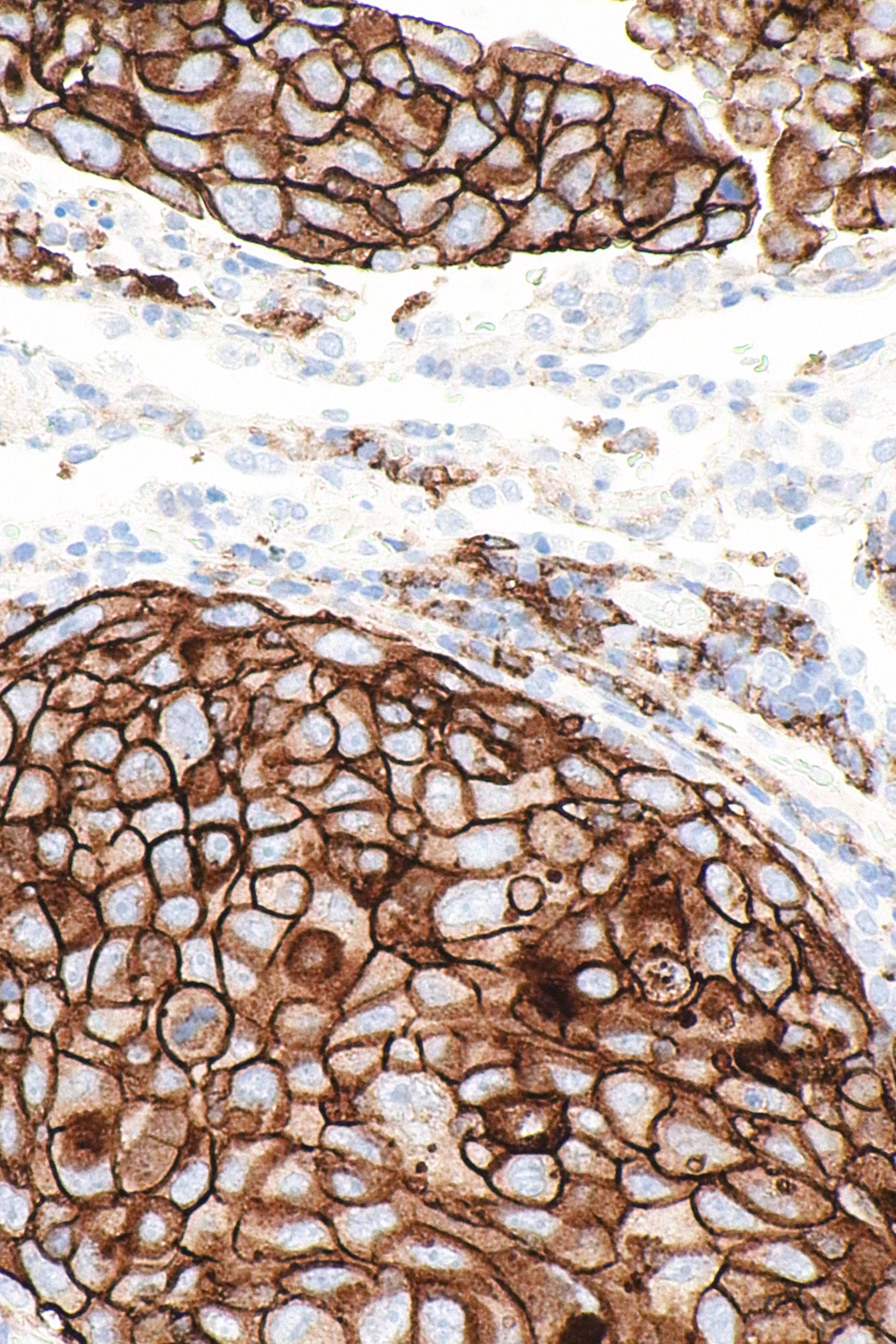
PD-1 inhibitörleri ve PD-L1 inhibitörleri nelerdir?
PD-1 inhibitörleri ve PD-L1 inhibitörleri, hücrelerin yüzeyinde bulunan PD-1 ve PDL1 immün kontrol noktası proteinlerinin aktivitesini bloke eden bir kontrol noktası inhibitörü antikanser ilaç grubudur. Bağışıklık kontrol noktası inhibitörleri, çeşitli kanser türleri için ön planda bir tedavi olarak ortaya çıkmaktadır.
PD-1 ve PD-L1 inhibitörleri, programlanmış ölüm ligandı 1’in (PD-L1) kendi reseptörü olan programlanmış hücre ölüm proteini 1 (PD-1) ile ilişkisini inhibe etme işlevi görür. Bu hücre yüzeyi proteinlerinin etkileşimi, bağışıklık sisteminin baskılanmasında rol oynar ve çevredeki konakçı hücrelerin öldürülmesini sınırlamak ve otoimmün hastalığı önlemek için enfeksiyonun ardından meydana gelir. Bu bağışıklık kontrol noktası, hamilelikte, doku allogreftlerinin ardından ve farklı kanser türlerinde de etkindir.
| İsim Soyisim | Hedef | Onaylandı |
|---|---|---|
| Nivolumab | PD-1 | 2014 |
| Pembrolizumab | PD-1 | 2014 |
| Atezolizumab | PD-L1 | 2016 |
| Avelumab | PD-L1 | 2017 |
| Durvalumab | PD-L1 | 2017 |
| Cemiplimab | PD-1 | 2018 |
Tarih
Kanserin tedavisi için PD-1 ve PD-L1’i bloke etme kavramı ilk olarak 2001 yılında yayınlandı. İlaç şirketleri bu molekülleri bloke etmek için ilaçlar geliştirmeye başladı ve ilk klinik çalışma 2006 yılında nivolumab’ı değerlendirerek başlatıldı. 2017 itibariyle, 20.000’den fazla hastada PD-1 ve PD-L1 inhibitörlerini içeren 500’den fazla klinik araştırma yapılmıştır. 2017’nin sonunda, PD-1 / PD-L1 inhibitörleri dokuz kanser türünün tedavisi için onaylandı.
Kanser immünoterapisi
Kanser hastalığı durumunda, tümör hücreleri üzerindeki PD-L1’in bir T hücresi üzerindeki PD-1 ile etkileşimi, bağışıklık sisteminin tümör hücrelerine saldırmasını önlemek için T hücresi fonksiyon sinyallerini azaltır. PD-L1’in PD-1 reseptörü ile etkileşimini bloke eden bir inhibitörün kullanılması, kanserin bu şekilde bağışıklık sisteminden kaçmasını önleyebilir. Klinikte, diğer kanser türlerinin yanı sıra, ilerlemiş melanom, küçük hücreli olmayan akciğer kanseri, renal hücreli karsinom, mesane kanseri ve Hodgkin lenfomada kullanılmak üzere birkaç PD-1 ve PD-L1 inhibitörü denenmektedir.
Bu immün kontrol noktası inhibitörleri ile immünoterapi, daha geniş bir tümör tipi yelpazesinde daha fazla sayıda hastada tümörleri küçültmektedir ve kalıcı yanıtlarla diğer immünoterapilere göre daha düşük toksisite seviyeleri ile ilişkilidir. Bununla birlikte, de-novo ve edinilmiş direnç hala hastaların büyük bir kısmında görülmektedir. Bu nedenle PD-L1 inhibitörleri, birçok farklı kanser için en umut verici ilaç kategorisi olarak kabul edilir.
Tüm hastalar PD-1 / PD-L1 inhibitörlerine yanıt vermez. FDA, bir inhibitöre tepki olasılığını tahmin etmek için tümör hücreleri tarafından ifade edilen PD-L1 seviyesini ölçmek için birkaç tahlili onayladı. PD-L1 seviyelerinin, tepkiyi yüksek oranda öngördüğü bulunmuştur. Daha yüksek mutasyon yükü, aynı zamanda anti-PD-1 / PD-L1 ajanlarına verilen yanıtın öngörücüsüdür.
PD-1 ve PD-L1 inhibitörleri, ipilimumab gibi CTLA4 (sitotoksik T-lenfosit ile ilişkili protein 4) inhibitörleri ile yakından ilişkilidir. PD-1 ve CTLA-4’ün her ikisi de aktive edilmiş T hücrelerinde ifade edilir, ancak bağışıklık tepkisinin farklı aşamalarında.
Mevcut klinik araştırmalar, anti-PD-1 ve PD-L1 ilaçlarını, LAG3, B7-H3, KIR, OX40, PARP, CD27 ve ICOS’u bloke eden diğer immünoterapi ilaçlarıyla kombinasyon halinde değerlendirmektedir.
Terapötikler
PD-1
Pembrolizumab (eski adıyla MK-3475 veya lambrolizumab, Keytruda) Merck tarafından geliştirilmiş ve ilk olarak 2014 yılında Gıda ve İlaç Dairesi tarafından melanom tedavisi için onaylanmıştır. Daha sonra metastatik küçük hücreli olmayan akciğer kanseri ve baş ve boyun skuamöz hücreli karsinomu için onaylandı. 2017 yılında, tümör bölgesinden ziyade tümörün genetik mutasyonlarına göre kullanım için onaylanan ilk immünoterapi ilacı oldu. Tümörlerinde eşanlamlı olmayan mutasyon yükü daha yüksek olan hastaların tedaviye daha iyi yanıt verdiği gösterilmiştir. Hem objektif yanıt oranları hem de progresyonsuz sağkalımlarının, eşanlamlı olmayan mutasyon yükü düşük olan hastalara göre daha yüksek olduğu gösterilmiştir.
Nivolumab (Opdivo), Bristol-Myers Squibb tarafından geliştirilmiş ve ilk olarak 2014 yılında FDA tarafından melanom tedavisi için onaylanmıştır. Daha sonra skuamöz hücreli akciğer kanseri, renal hücreli karsinom ve Hodgkin lenfoma için onaylandı.
Cemiplimab (Libtayo), Regeneron Pharmaceuticals tarafından geliştirildi ve ilk olarak 2018 yılında FDA tarafından küratif cerrahi veya küratif radyasyon için aday olmayan kutanöz skuamöz hücreli karsinom (CSCC) veya yerel olarak gelişmiş CSCC’nin tedavisi için onaylandı.
Deneysel
Şu anda, birçok PD-1 inhibitörü geliştirme aşamasındadır:
- Jounce Therapeutics tarafından JTX-4014 2020 itibariyle Faz I denemesine girdi
- Spartalizumab (PDR001), Novartis tarafından hem katı tümörleri hem de lenfomaları tedavi etmek için geliştirilen ve 2018 itibariyle Faz III denemelerine giren bir PD-1 inhibitörüdür.
- Camrelizumab (SHR1210), Jiangsu HengRui Medicine Co., Ltd. tarafından piyasaya sürülen ve nükseden veya refrakter klasik Hodgkin lenfoma tedavisi için yakın zamanda Çin’de şartlı onay alan bir anti-PD-1 monoklonal antikorudur.
- Innovent ve Eli Lilly tarafından küçük hücreli olmayan akciğer kanseri (NSCLC) olan hastalar için geliştirilmiş bir insan anti-PD-1 antikoru olan Sintilimab (IBI308).
- Tislelizumab (BGB-A317), katı tümörler ve hematolojik kanserlerde önemli Faz 3 ve Faz 2 klinik deneylerinde insanlaştırılmış bir IgG4 anti-PD-1 monoklonal antikordur.
- Toripalimab (JS 001), klinik araştırma altında PD-1’e karşı insanlaştırılmış bir IgG4 monoklonal antikordur.
- Dostarlimab (TSR-042, WBP-285), GlaxoSmithKline tarafından araştırılan PD-1’e karşı insanlaştırılmış bir monoklonal antikordur.
- INCMGA00012 (MGA012), Incyte ve MacroGenics tarafından geliştirilmiş bir insanlaştırılmış IgG4 monoklonal antikorudur.
- AMP-224, AstraZeneca / MedImmune ve GlaxoSmithKline tarafından
- AMP-514 (MEDI0680), AstraZeneca
PD-L1
Atezolizumab (Tecentriq), Roche Genentech tarafından geliştirilmiş tamamen insanlaştırılmış bir IgG1 (immünoglobulin 1) antikorudur. 2016 yılında FDA, ürotelyal karsinom ve küçük hücreli olmayan akciğer kanseri için atezolizumab’ı onayladı.
Avelumab (Bavencio), Merck Serono ve Pfizer tarafından geliştirilmiş tamamen insan IgG1 antikorudur. Avelumab, metastatik merkel hücreli karsinomun tedavisi için FDA onaylıdır. Mide kanseri için Faz III klinik denemelerinde başarısız oldu.
Durvalumab (Imfinzi), AstraZeneca tarafından geliştirilmiş tamamen insan IgG1 antikorudur. Durvalumab, kemoradyasyondan sonra ürotelyal karsinom ve rezeke edilemeyen küçük hücreli dışı akciğer kanserinin tedavisi için FDA onaylıdır.
Deneysel
En az iki PD-L1 inhibitörü, geliştirmenin deneysel aşamasındadır.
- KN035 şu anda ABD, Çin ve Japonya’da klinik değerlendirmeler altında olan deri altı formülasyonlu tek PD-L1 antikorudur
- Checkpoint Therapeutics tarafından CK-301
- AUNP12 Aurigene ve Laboratoires Pierre Fabre tarafından geliştirilen ilk peptik PD-1 / PD-L1 inhibitörü olarak 29 mer’lik bir peptittir ve umut vaat eden bir klinik deneyde değerlendirilmektedir. içinde vitro Sonuçlar.
- CA-170, Aurigene / Curis tarafından PD-L1 ve VISTA antagonisti olarak keşfedilen, güçlü bir küçük molekül inhibitörü olarak suçlandı. laboratuvar ortamında. Bu nedenle, bileşik şu anda mezotelyoma hastaları üzerinde faz I klinik deneme altındadır.
- BMS-986189 Bristol-Myers Squibb tarafından keşfedilen ve farmakokinetiği, güvenliği ve tolere edilebilirliği şu anda sağlıklı denekler üzerinde çalışılan makrosiklik bir peptiddir.
Yan etkiler
Grup olarak immünoterapilerin hedef dışı etkileri ve kendilerine özgü toksisiteleri vardır. Bunlardan bazıları, interstisyel pnömonit, kolit, hepatit, tiroidit, deri reaksiyonları, düşük trombosit ve beyaz kan hücreleri seviyeleri, beyin veya omurilik iltihabı, miyozit dahil nöromüsküler advers olaylar, Guillain-Barré sendromu, miyastenia gravis; miyokardit ve kalp yetmezliği, akut adrenal yetmezlik ve nefrit. Böbreklerle ilgili en yaygın değişiklikler akut interstisyel nefrittir, bunu glomerüler hastalıklar ve ardından tübüler hasar izler. Bu yan etkilerin ayrıntılı mekanizması tam olarak açıklanmamıştır; ancak, bilinen otoimmün hastalıklardan açıkça farklıdırlar. Bağışıklık aracılı advers reaksiyonlar genellikle T hücrelerinin genelleştirilmiş düzensizliğine veya otoantikorların gelişimine atfedilir, ancak gizli viral enfeksiyonlara karşı hafıza T hücresi yanıtları, kombine PD-1 / CTLA-4 blokajını takiben ilerlemiş melanomlu bazı hastalarda da rol oynayabilir.
Standart kemoterapötik ajanlarla karşılaştırıldığında, PD-1 / PD-L1 inhibitörleri daha düşük yorgunluk, duyusal nöropati, diyare, kemik iliği baskılanması, iştahsızlık, mide bulantısı ve kabızlık vakalarına sahipti.
.











:max_bytes(150000):strip_icc()/GettyImages-146272894-ed61213bad9c476ea00233feb7e7729f.jpg)
:max_bytes(150000):strip_icc()/surgeon-GettyImages-200140323-001-578ce4ab5f9b584d20ce3d9f.jpg)
Discussion about this post