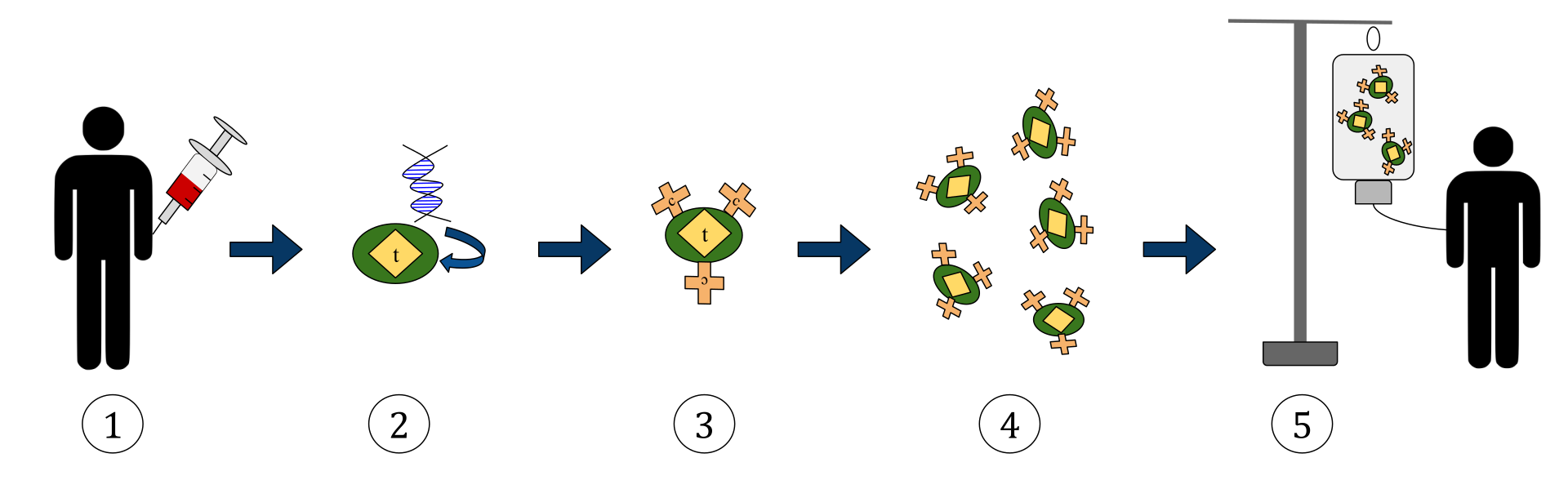
Yukarıdaki diyagram, kimerik antijen reseptörü T-hücresi terapisi (CAR) sürecini temsil etmektedir. Bu, kanser tedavisinde giderek büyüyen bir uygulama olan bir immünoterapi yöntemidir. Nihai sonuç, vücuttaki enfekte kanser hücrelerini tanıyabilen ve bunlarla savaşabilen donanımlı T hücrelerinin üretimi olmalıdır.
1. T hücreleri (‘t’ olarak etiketlenen nesnelerle temsil edilir) hastanın kanından çıkarılır.
2. Daha sonra bir laboratuar ortamında, spesifik antijen reseptörlerini kodlayan gen, T hücrelerine dahil edilir.
3. Böylece hücrelerin yüzeyinde CAR reseptörlerini (c olarak etiketlenir) üretir.
4. Yeni modifiye edilmiş T hücreleri daha sonra laboratuarda toplanır ve büyütülür.
5. Belirli bir süre sonra, tasarlanmış T-hücreleri hastaya geri infüze edilir.
Kimerik antijen reseptörü T hücreleri (Ayrıca şöyle bilinir CAR T hücreleri) immünoterapide kullanılmak üzere yapay bir T hücresi reseptörü üretmek için genetik olarak tasarlanmış T hücreleridir.
Kimerik antijen reseptörleri (Arabalar, Ayrıca şöyle bilinir kimerik immünoreseptörler, kimerik T hücre reseptörleriveya yapay T hücre reseptörleri) T hücrelerine belirli bir proteini hedefleme konusunda yeni bir yetenek kazandırmak için tasarlanmış reseptör proteinleridir. Reseptörler kimeriktir çünkü hem antijen bağlayıcı hem de T hücresi aktive edici fonksiyonları tek bir reseptörde birleştirirler.
CAR-T hücre tedavisi, kanser tedavisi için CAR’lar ile tasarlanmış T hücrelerini kullanır. CAR-T immünoterapisinin öncülü, daha etkili bir şekilde hedeflemek ve yok etmek için T hücrelerini kanser hücrelerini tanımak üzere modifiye etmektir. Bilim adamları, insanlardan T hücrelerini toplar, genetik olarak değiştirirler ve daha sonra ortaya çıkan CAR-T hücrelerini, tümörlerine saldırmak için hastalara aşılarlar. CAR-T hücreleri, bir hastanın kendi kanındaki (otolog) T hücrelerinden türetilebilir veya başka bir sağlıklı vericinin T hücrelerinden (allojenik) türetilebilir. Bir kişiden izole edildikten sonra, bu T hücreleri, onları tümörlerin yüzeyinde bulunan bir antijeni hedef alacak şekilde programlayan belirli bir BAB’yi ifade edecek şekilde genetik olarak tasarlanmıştır. Güvenlik için CAR-T hücreleri, sağlıklı hücrelerde eksprese edilmeyen bir tümörde eksprese edilen bir antijene spesifik olacak şekilde tasarlanmıştır.
CAR-T hücreleri bir hastaya infüze edildikten sonra, kanser hücrelerine karşı “canlı bir ilaç” görevi görürler. Bir hücrede hedeflenen antijeni ile temas ettiklerinde, CAR-T hücreleri ona bağlanır ve aktive olur, ardından çoğalmaya ve sitotoksik hale gelir. CAR-T hücreleri hücreleri, yoğun uyarılmış hücre proliferasyonu, diğer canlı hücrelere toksik olma derecesini arttırma (sitotoksisite) ve sitokinler, interlökinler gibi diğer hücreleri etkileyebilecek faktörlerin salgılanmasının artmasına neden olarak dahil olmak üzere çeşitli mekanizmalar yoluyla yok eder. büyüme faktörleri.
CAR-T hücrelerinin üretimi

CAR-T hücrelerinin üretimindeki ilk adım, T hücrelerinin insan kanından izole edilmesidir. CAR-T hücreleri, otolog tedavi olarak bilinen hastanın kendi kanından veya allojenik tedavi olarak bilinen sağlıklı bir donörün kanından üretilebilir. Her iki durumda da üretim süreci aynıdır; sadece ilk kan vericisinin seçimi farklıdır.
İlk olarak, lökositler, lökosit aferezi olarak bilinen bir işlemde bir kan hücresi ayırıcısı kullanılarak izole edilir. Periferal kan mononükleer hücreleri (PBMC) daha sonra ayrılır ve toplanır. Lökosit aferezinin ürünleri daha sonra bir hücre işleme merkezine aktarılır. Hücre işleme merkezinde, spesifik T hücreleri uyarılır, böylece aktif olarak çoğalır ve büyük sayılara genişler. Genişlemelerini sağlamak için, T hücreleri tipik olarak sitokin interlökin 2 (IL-2) ve anti-CD3 antikorları ile tedavi edilir.
Genişletilmiş T hücreleri saflaştırılır ve daha sonra, bir retroviral vektör yoluyla, tipik olarak bir entegre gamaretrovirüs (RV) veya bir lentiviral (LV) vektör olmak üzere tasarlanmış CAR’yi kodlayan bir gen ile transdüksiyona tabi tutulur. Bu vektörler, U3 bölgesinin kısmen silinmesi nedeniyle modern zamanlarda çok güvenlidir. CAR genini genomdaki belirli bölgelere entegre etmek için son zamanlarda retroviral vektörler yerine yeni gen düzenleme aracı CRISPR / Cas9 kullanıldı.
Hasta, tasarlanmış CAR-T hücrelerinin eklenmesinden önce lenfodeplesiyon kemoterapisine tabi tutulur. Hastada dolaşımdaki lökosit sayısının azalması, üretilen sitokinlerin sayısını artırır ve kaynaklar için rekabeti azaltır, bu da tasarlanmış CAR-T hücrelerinin genişlemesini teşvik etmeye yardımcı olur.
Klinik uygulamalar
Mart 2019 itibariyle, dünya çapında CAR-T hücrelerini içeren yaklaşık 364 devam eden klinik çalışma vardı. Bu denemelerin çoğu kan kanserlerini hedeflemektedir: CAR-T tedavileri, hematolojik maligniteler için yapılan tüm denemelerin yarısından fazlasını oluşturmaktadır. CD19, en popüler antijen hedefi olmaya devam ediyor, ardından BCMA (genellikle multipl miyelomda ifade edilir). 2016 yılında, çalışmalar CD20 gibi diğer antijenlerin canlılığını keşfetmeye başladı. Katı tümör denemelerine CAR-T daha az hakimdir ve hücre terapisine dayalı denemelerin yaklaşık yarısı NK hücreleri gibi diğer platformları içerir.
Kanser
T hücreleri, spesifik olarak bir hastanın tümör hücrelerindeki antijenlere yönelik kimerik antijen reseptörlerini eksprese etmek üzere genetik olarak tasarlanmıştır ve daha sonra, kanser hücrelerine saldırıp onları öldürdükleri hastaya aşılanır. CAR ile modifiye edilmiş T hücreleri, hemen hemen tüm tümörle ilişkili antijeni hedef alacak şekilde tasarlanabilir.
Erken CAR-T hücre araştırmaları kan kanserleri üzerine odaklandı. İlk onaylanmış tedaviler, akut lenfoblastik lösemi (ALL) ve diffüz büyük B hücreli lenfoma (DLBCL) gibi B hücresinden türetilmiş kanserlerde bulunan antijen CD19’u hedefleyen CAR’leri kullanır. Refrakter Hodgkin lenfomasında CD30 da dahil olmak üzere diğer birçok kan kanseri antijenini hedefleyen CAR’lerin tasarlanması için çalışmalar devam etmektedir; Akut miyeloid lösemide (AML) CD33, CD123 ve FLT3; ve multipl miyelomda BCMA.
Solid tümörler daha zor bir hedef oluşturdu. İyi antijenlerin tanımlanması zor olmuştur: bu tür antijenler, kanser hücrelerinin çoğunda yüksek oranda ifade edilmeli, ancak normal dokularda büyük ölçüde bulunmamalıdır. CAR-T hücreleri ayrıca katı tümör kütlelerinin merkezine etkili bir şekilde trafiğe sokulmaz ve düşman tümör mikro ortamı, T hücresi aktivitesini baskılar.
Otoimmün rahatsızlığı
Çoğu CAR T hücresi çalışması, belirli bir hücre popülasyonunu (örneğin, lenfoma hücrelerini hedefleyen CAR T hücreleri) ortadan kaldırabilen bir CAR T hücresi oluşturmaya odaklanırken, bu teknolojinin başka potansiyel kullanımları da vardır. T hücreleri ayrıca kendi antijenlerini otoimmün reaksiyonlardan koruyabilir. Bir CAR ile donatılmış düzenleyici bir T hücresi, belirli bir antijene tolerans verme potansiyeline sahip olabilir, bu, organ naklinde veya lupus gibi romatizmal hastalıklarda kullanılabilecek bir şey olabilir.
Satefy
CAR-T hücrelerinin vücuda girmesinden kaynaklanan, sitokin salınım sendromu ve nörolojik toksisite dahil olmak üzere ciddi yan etkiler vardır. Nispeten yeni bir tedavi olduğu için, CAR-T hücre tedavisinin uzun vadeli etkileri hakkında çok az veri vardır. CAR-T hücreleri ile tedavi edilen kadın hastalarda uzun süreli hasta sağkalımı ve gebelik komplikasyonları hakkında hala endişeler var. Anafilaksi beklenen bir yan etkidir, çünkü CAR yabancı bir monoklonal antikor ile yapılır ve sonuç olarak bir bağışıklık tepkisi tetikler.
Hedefte / tümör dışı tanıma, CAR-T hücresi doğru antijeni tanıdığında gerçekleşir, ancak antijen sağlıklı, patojenik olmayan doku üzerinde ifade edilir. Bu, CAR-T hücrelerinin, CD19 eksprese eden sağlıklı B hücreleri gibi tümör dışı dokulara saldırmasıyla sonuçlanır. Bu yan etkinin şiddeti, destekleyici infüzyonlarla tedavi edilebilen B hücresi aplazisinden ölüme yol açan aşırı toksisiteye kadar değişebilir.
Ayrıca, CAR genini konakçı T hücresinin genomundaki bir tümör baskılayıcıya veya onkojene sokan viral vektör nedeniyle, tasarlanmış CAR-T hücrelerinin, insersiyonel mutajenez yoluyla kanserli hücrelere dönüşme olasılığı da düşüktür. Bazı retroviral (RV) vektörler, lentiviral (LV) vektörlerden daha düşük risk taşır. Bununla birlikte, her ikisinin de onkojenik olma potansiyeli vardır. CAR T hücresi fonksiyonunun ve in vivo kalıcılığının daha iyi anlaşılması için T hücrelerinde CAR ekleme bölgelerinin genomik sekanslama analizi oluşturulmuştur.
Sitokin salıverilme sendromu
CAR-T hücreleriyle tedaviden sonra en yaygın sorun, bağışıklık sisteminin aktive olduğu ve artan sayıda inflamatuar sitokin saldığı bir durum olan sitokin salım sendromudur (CRS). Bu sendromun klinik görünümü, yüksek ateş, yorgunluk, miyalji, mide bulantısı, kılcal sızıntılar, taşikardi ve diğer kardiyak disfonksiyon, karaciğer yetmezliği ve böbrek yetmezliğiyle birlikte sepsise benzer. KRS, CAR-T hücre tedavisi ile tedavi edilen hemen hemen tüm hastalarda ortaya çıkar; aslında, CRS’nin varlığı, CAR-T hücrelerinin kanser hücrelerini öldürmek için tasarlandığı şekilde çalıştığını gösteren bir tanısal belirteçtir. Bununla birlikte, daha yüksek bir KRS şiddeti derecesinin tedaviye artan yanıtla ilişkili olmadığını, daha çok daha yüksek hastalık yükü ile ilişkili olduğunu unutmayın.
Bağışıklık efektör hücre ile ilişkili nörotoksisite
Nörolojik toksisite ayrıca sıklıkla CAR-T hücre tedavisi ile ilişkilidir. Altta yatan mekanizma yeterince anlaşılmamıştır ve KRS ile ilişkili olabilir veya olmayabilir. Klinik belirtiler arasında deliryum, hala dili yorumlama yeteneğine sahipken tutarlı bir şekilde konuşma yeteneğinin kısmi kaybı (ifade edici afazi), azalmış uyanıklık (obtundation) ve nöbetler yer alır. Bazı klinik denemeler sırasında nörotoksisitenin neden olduğu ölümler meydana geldi. Nörotoksisiteden kaynaklanan ana ölüm nedeni serebral ödemdir. Juno Therapeutics, Inc. tarafından yapılan bir çalışmada, denemeye katılan beş hasta beyin ödemi nedeniyle öldü. Hastalardan ikisi tek başına siklofosfamid ile tedavi edildi ve geri kalan üçü bir siklofosfamid ve fludarabin kombinasyonu ile tedavi edildi. Fred Hutchinson Kanser Araştırma Merkezi tarafından desteklenen başka bir klinik çalışmada, CAR-T hücrelerinin uygulanmasından 122 gün sonra geri döndürülemez ve ölümcül nörolojik toksisite vakası bildirilmiştir.
.









:max_bytes(150000):strip_icc()/GettyImages-83637854-594491fd5f9b58d58a8e1be8.jpg)

Discussion about this post